Las versiones defectuosas del gen Foxp2 interrumpen la capacidad de las neuronas para formar sinapsis en las regiones del cerebro involucradas en el habla, muestra un nuevo estudio.
Las mutaciones de un gen llamado Foxp2 se han relacionado con un tipo de trastorno del habla llamado apraxia que dificulta la producción de secuencias de sonido. Un nuevo estudio del MIT y la Universidad Nacional Yang Ming Chiao Tung arroja luz sobre cómo este gen controla la capacidad de producir el habla.
En un estudio con ratones, los investigadores encontraron que las mutaciones en Foxp2 interrumpen la formación de dendritas y sinapsis neuronales en el cuerpo estriado del cerebro, que desempeña funciones importantes en el control del movimiento. Los ratones con estas mutaciones también mostraron deficiencias en su capacidad para producir los sonidos de alta frecuencia que utilizan para comunicarse con otros ratones.
Esas disfunciones surgen porque las mutaciones de Foxp2 impiden el ensamblaje adecuado de las proteínas motoras, que mueven las moléculas dentro de las células, encontraron los investigadores.
“Estos ratones tienen vocalizaciones anormales y en el cuerpo estriado hay muchas anomalías celulares“, dice Ann Graybiel, profesora del Instituto MIT, miembro del Instituto McGovern para la Investigación del Cerebro del MIT y autora del artículo. “Este fue un hallazgo emocionante. ¿Quién hubiera pensado que un problema del habla podría provenir de pequeños motores dentro de las células?“
Fu-Chin Liu PhD ’91, profesor de la Universidad Nacional Yang Ming Chiao Tung en Taiwán, es el autor principal del estudio, que aparece en la revista Brain. Liu y Graybiel también trabajaron juntos en un estudio de 2016 sobre el vínculo potencial entre Foxp2 y el autismo. Los autores principales del nuevo artículo de Brain son Hsiao-Ying Kuo y Shih-Yun Chen de la Universidad Nacional Yang Ming Chiao Tung.
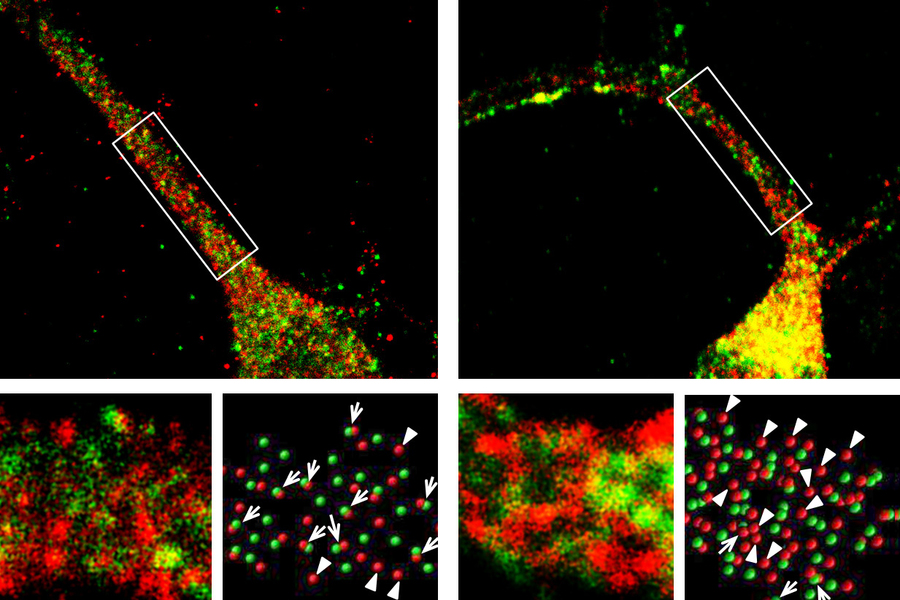
Control de voz
Los niños con apraxia asociada con Foxp2 tienden a comenzar a hablar más tarde que otros niños y su habla suele ser difícil de entender. Se cree que el trastorno surge de deficiencias en las regiones del cerebro, como el cuerpo estriado, que controlan los movimientos de los labios, la boca y la lengua. El Foxp2 también se expresa en el cerebro de pájaros cantores como los pinzones cebra y es fundamental para la capacidad de esos pájaros para aprender canciones.
El Foxp2 codifica un factor de transcripción, lo que significa que puede controlar la expresión de muchos otros genes diana. Muchas especies expresan Foxp2, pero los humanos tienen una forma especial de Foxp2. En un estudio de 2014, Graybiel y sus colegas encontraron evidencia de que la forma humana de Foxp2, cuando se expresaba en ratones, les permitía acelerar el cambio de tipos de aprendizaje declarativo a procedimental.
En ese estudio, los investigadores demostraron que los ratones diseñados para expresar la versión humana de Foxp2, que difiere de la versión del ratón en solo dos pares de bases de ADN, eran mucho mejores para aprender laberintos y realizar otras tareas que requieren convertir acciones repetidas en rutinas de comportamiento. Los ratones con Foxp2 similar a los humanos también tenían dendritas más largas, las extensiones delgadas que ayudan a las neuronas a formar sinapsis, en el cuerpo estriado, que está involucrado en la formación de hábitos y en el control motor.
En el nuevo estudio, los investigadores querían explorar cómo la mutación Foxp2 que se ha relacionado con la apraxia afecta la producción del habla, usando vocalizaciones ultrasónicas en ratones como un representante del habla. Muchos roedores y otros animales, como los murciélagos, producen estas vocalizaciones para comunicarse entre sí.
Si bien estudios previos, incluido el trabajo de Liu y Graybiel en 2016, habían sugerido que Foxp2 afecta el crecimiento de las dendritas y la formación de sinapsis, se desconocía el mecanismo por el que esto ocurre. En el nuevo estudio, dirigido por Liu, los investigadores investigaron un mecanismo propuesto, que es que Foxp2 afecta a las proteínas motoras.
Uno de estos motores moleculares es el complejo de proteína dineína, un gran grupo de proteínas que es responsable de transportar moléculas a lo largo de los andamios de microtúbulos dentro de las células.
“Todo tipo de moléculas se desvían a diferentes lugares de nuestras células, y eso es ciertamente cierto en el caso de las neuronas“, dice Graybiel. “Hay un ejército de moléculas diminutas que mueven moléculas en el citoplasma o las colocan en la membrana. En una neurona, pueden enviar moléculas desde el cuerpo celular hasta los axones“.
Un delicado equilibrio
El complejo de dineína se compone de varias otras proteínas. El más importante de ellos es una proteína llamada dynactin1, que interactúa con los microtúbulos, lo que permite que el motor de la dineína se mueva a lo largo de los microtúbulos. En el nuevo estudio, los investigadores encontraron que dynactin1 es uno de los principales objetivos del factor de transcripción Foxp2.
Los investigadores se centraron en el cuerpo estriado, una de las regiones donde Foxp2 se encuentra con mayor frecuencia, y demostraron que la versión mutada de Foxp2 no puede suprimir la producción de dynactin1. Sin ese freno, las células generan demasiada dinactina1. Esto altera el delicado equilibrio de la dineína-dinactina1, que impide que el motor de la dineína se mueva a lo largo de los microtúbulos.
Esos motores son necesarios para transportar moléculas que son necesarias para el crecimiento de las dendritas y la formación de sinapsis en las dendritas. Con esas moléculas varadas en el cuerpo celular, las neuronas no pueden formar sinapsis para generar las señales electrofisiológicas adecuadas que necesitan para hacer posible la producción del habla.
Los ratones con la versión mutada de Foxp2 tenían vocalizaciones ultrasónicas anormales, que suelen tener una frecuencia de alrededor de 22 a 50 kilohercios. Los investigadores demostraron que podían revertir estas alteraciones de la vocalización y los déficits en la actividad motora molecular, el crecimiento dendrítico y la actividad electrofisiológica al rechazar el gen que codifica la dynactin1.
Las mutaciones de Foxp2 también pueden contribuir al autismo y la enfermedad de Huntington, a través de mecanismos que Liu y Graybiel estudiaron previamente en su artículo de 2016 y que ahora están explorando muchos otros grupos de investigación. El laboratorio de Liu también está investigando el papel potencial de la expresión anormal de Foxp2 en el núcleo subtalámico del cerebro como un posible factor en la enfermedad de Parkinson.
Bibliografía:
Hsiao-Ying Kuo, Shih-Yun Chen, Rui-Chi Huang, Hiroshi Takahashi, Yen-Hui Lee, Hao-Yu Pang, Cheng-Hsi Wu, Ann M Graybiel, Fu-Chin Liu, Speech- and language-linked FOXP2 mutation targets protein motors in striatal neurons, Brain, 2023;, awad090, https://doi.org/10.1093/brain/awad090
Nota de prensa del Massachusetts Institute of Technology. Original escrito por Anne Trafton. Nota: el contenido se puede editar por estilo y longitud.
Descubre más desde Autismo Diario
Suscríbete y recibe las últimas entradas en tu correo electrónico.





